Atomin viimeisen eli uloimman elektronikuoren rakenne määrittää sen, miten aine reagoi muiden aineiden kanssa. Uloimmalla elektronikuorella voi olla 1-8 elektronia. Kun atomin uloimmalla elektronikuorella on 8 elektronia, sanotaan että sillä on oktetti.
Esimerkiksi neonilla (Ne) on oktetti:
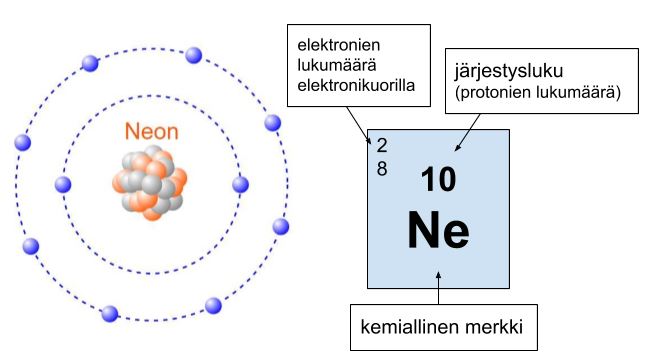
Neonin uloimmalla elektronikuorella on 8 elektronia. Neonilla on siis oktetti.
Ensimmäiselle elektronikuorelle mahtuu vain kaksi elektronia. Vedyllä ja heliumilla on vain yksi elektronikuori. Vedyllä on vain yksi elektroni, mutta heliumilla on kaksi elektronia. Kun atomilla on yksi elektronikuori ja siinä kaksi elektronia, sanotaan että atomilla on pikkuoktetti. Heliumilla on siis pikkuoktetti.
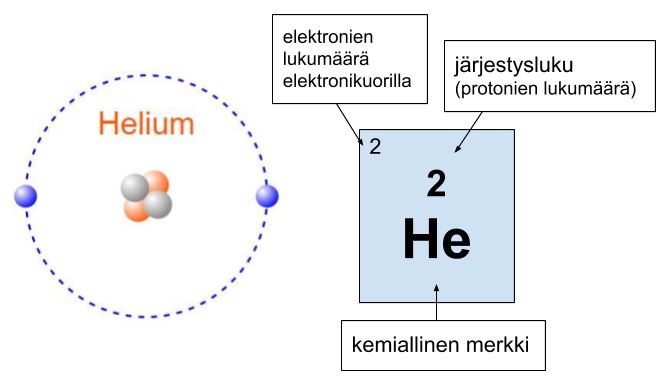
Heliumilla on vain yksi elektronikuori ja siinä kaksi elektronia. Elektronikuori on siis täysi ja heliumilla on pikkuoktetti.
Alkuaineet reagoivat luovuttamalla tai vastaanottamalla elektroneja. Atomit pyrkivät saavuttamaan oktetin, koska oktetti on hyvin pysyvä rakenne. Jos alkuaineella on oktetti tai pikkuoktetti, se ei reagoi helposti muiden aineiden kanssa.
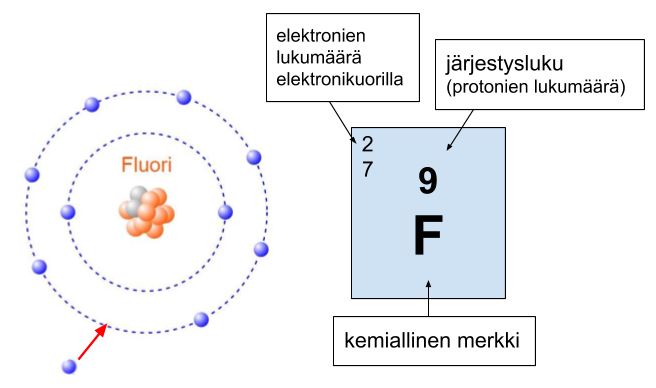
Jos atomilla on 5-7 ulkoelektronia, se vastaanottaa mielellään elektroneja. Atomin tavoitteena on saavuttaa oktettirakenne. Fluoriatomilla (F) on 7 ulkoelektronia. Se haluaa vastaanottaa yhden elektronin.
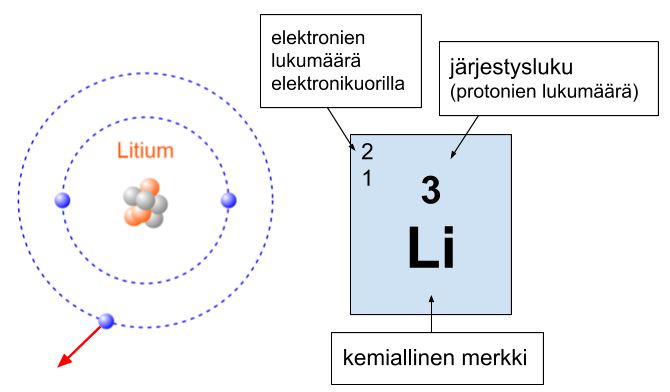
Jos atomilla on 1-3 ulkoelektronia, se luovuttaa ne mielellään pois. Litiumilla (Li) on yksi ulkoelektroni. Litium haluaa luovuttaa ulkoelektronin pois.
Tutki jaksollista järjestelmää ja vastaa kysymyksiin. Jaksollisen järjestelmän löydät kemian oppikirjasta tai esimerkiksi täältä: https://www.ptable.com/?lang=fi